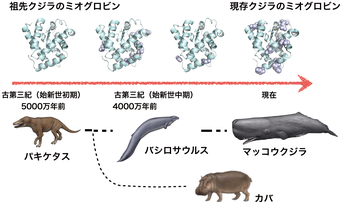
本学生命科学部の今村比呂志(ひろし)助教は、他大学の研究者と共同でクジラの筋細胞タンパク質ミオグロビン(Mb)からクジラの祖先のMbを推定し、復元することに成功した。Mbは筋肉中で酸素を貯蔵する。祖先クジラのMbと現存するマッコウクジラのMbを比較することで、クジラのMbの進化過程が解明された。
期待されるバイオ医薬への応用
クジラの先祖パキケタスが現在のマッコウクジラに至るまでには陸棲から水棲へ、そして浅い海から深い海へという2種類の大きな進化があり、それぞれに必要なMb性質は異なることが解明された。前者の過程ではMbの電気的な性質が変化し、筋細胞内で沈殿しにくくなった。よってMbの周りが分子で囲まれていても溶解でき、動ける性質を獲得した。また後者の過程で、Mbはコンパクトにまとまる性質を示すようになり、Mb同士が結合しにくくなったことで、それ自体の機能向上が認められた。
今回の研究によって期待されるのが、バイオ医薬品への応用だ。薬の性質はそれぞれのタンパク質が個として分散することで発揮されるものであるが、タンパク質同士が結合するとその機能が失われてしまうことがある。本庶佑氏のノーベル賞受賞で抗がん剤オプジーボが脚光を浴びたとはいえ、タンパク質医薬品にはこうした複雑な機構が存在し、依然として100㎎あたり数十万円もの高値で販売されているのが現状だ。人間とクジラのタンパク質の類似性およびタンパク質同士の結合性などを解明することで、医薬品開発費の低減が期待でき、結果として安価に医薬品を供給できるようになる。
今村助教は今後の研究課題を「電気的な性質だけでなく、なぜMb同士が結合しないでいられるのかを物理化学的な観点からも解明したい。また、クジラだけでなくアザラシが持つMbの構造の安定性と結合性の関係についても明らかにしたい」と語り、さらなる構造解明に意欲を示した。(花田)

コメントをお書きください